TMB版图扩张,进军结直肠癌免疫治疗
肿瘤突变负荷(Tumor Mutational Burden, TMB)定义为肿瘤基因组中每Mb的突变数量,最早于2014-2015年由纪念斯隆-凯特琳癌症中心(Memorial Sloan Kettering Cancer Center, MSKCC)的TA Chan研究组提出[1,2]。科学家们发现,TMB水平高的患者对于免疫检查点抑制剂治疗的响应更好,是免疫治疗的潜在生物标志物。

图1 TMB诞生的两篇论文
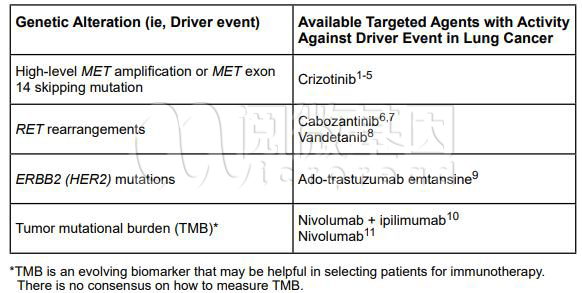
从提出到现在短短4、5年时间里,关于TMB的研究飞速发展,成果不断涌现。尤其是在肺癌领域,随着大量研究证明TMB与PD-1抗体疗效之间的关系,2019年第5版NCCN非小细胞肺癌指南已将TMB作为新兴生物标志物纳入指南[3]。
图2 NCCN非小细胞肺癌指南2019第5版——新兴生物标志物
随着研究的深入,TMB在其它癌种中的预后及预测作用研究报道也开始涌现。今天,大阅哥先带大家来看一看近期TMB在结直肠癌领域的新进展。
第一篇论文来自Federico Innocenti博士领导的团队,报道了TMB是结直肠癌的预后指标[4],相关研究于3月13日发表于Journal of Clinical Oncology。本研究共纳入843名患者样本进行分子标志物检测,患者均来自CALGB/SWOG 80405三期临床实验。
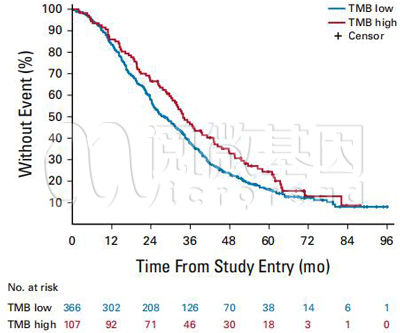
同过去研究较为一致,本研究中携带KRAS/NRAS/BRAF突变的患者总生存期减短。此三种突变均为野生型的患者中位OS为35.9个月,而携带至少一个基因突变的中位OS为22.2个月(P < 0.001);MSI-H型的患者接受一线化疗加贝伐珠单抗总生存期优于一线接受化疗加西妥西单抗的MSI-H型患者(HR = 0.13 [95% CI, 0.06 ~ 0.30], MSI状态与两种治疗方法之间存在显著的交互作用, P<0.001);并且,他们发现TMB-H的患者较之TMB-L的患者拥有更长的总生存期(HR = 0.73, [95%CI, 0.57 ~ 0.95], P = 0.02 )。
图3 TMB-H患者拥有更长的OS (引自[4])
虽然预后方面两组差异看起来不是非常显著,不过更令人惊喜的是在免疫治疗疗效预测方面。
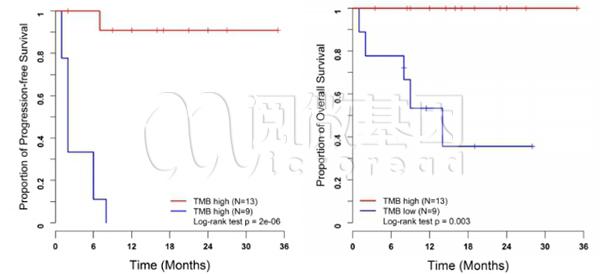
来自Marwan Fakih博士领导研究团队,报道了在MSI-H型结直肠癌患者中,TMB-H患者较TMB-L患者更能够从PD-1/PD-L1抗体治疗中获益[5],相关研究于4月30日发表于Annals of Oncology。研究纳入了22名经免疫检查点抑制剂治疗的MSI-H患者,其中19人使用的是帕博利珠单抗(Keytruda)。经panel测序获得其TMB值,本研究中TMB的阈值经计算为37~41 突变/Mb。全部13名TMB-H患者达到CR/PR,而6/9名TMB-L患者病情进展。TMB-H患者中未达到中位PFS(中位随访时间18个月),而TMB-L患者中位PFS仅为2个月( HR = 0.03, [95%CI, 0.003~0.23], P = 0.00087 )。进一步分析表明,将OS作为评价标准,TMB同样是免疫检查点抑制剂治疗的疗效预测标志物。
为保证本研究中所得的TMB阈值具有一定的普遍性,研究者进一步分析了Foundation Medicine的数据库。在18,140份数据中,共有821名MSI-H患者(4.5%),其中位TMB为46.1 突变/Mb,而MSS患者的中位TMB仅为3.5 突变/Mb。本研究MSI-H患者中位TMB为46.5 突变/Mb,与数据库记载相似。本研究中计算所得37~41的阈值大致对应于数据库MSI-H患者TMB的35%分位数。因此,研究团队推荐结直肠癌MSI-H型患者的TMB阈值可以取35%分位数作界限。
图4 以PFS(左)和OS(右)作为评价标准,TMB都是MSI-H型患者中免疫检查点抑制剂治疗的疗效预测指标。本研究中TMB的预测计算为37~41
我们惊喜的看到TMB这个潜力无限的新兴标志物走出了肺癌领域,开始在更多癌种中发挥它指导精准医疗的强大预后、预测能力。尤其是第二项研究中,我们看到TMB能够作为MSI检测的强有力补充,更为准确的找到适合免疫治疗的患者。当然,由于该研究纳入的患者有限,我们还需要更多的真实世界数据验证这一发现。我们也期盼有兴趣的老师和我们联系,共同推进TMB在结直肠癌等领域的不断发展。
参考文献:
1. Snyder, A., et al. (2014). Genetic basis for clinical response to CTLA-4 blockade in melanoma. New England Journal of Medicine.DOI: 10.1056/NEJMoa1406498
2. Rizvi, N. A., et al. (2015). Mutational landscape determines sensitivity to PD-1 blockade in non–small cell lung cancer. Science. DOI: 10.1126/science.aaa1348
3. National Comprehensive Cancer Network. Non-Small Cell Lung Cancer (Version 5.2019).Accessed June 18, 2019.
4. Innocenti, F., et al. (2019). Mutational Analysis of Patients With Colorectal Cancer in CALGB/SWOG 80405 Identifies New Roles of Microsatellite Instability and Tumor Mutational Burden for Patient Outcome. Journal of Clinical Oncology. DOI: 10.1200/JCO.18.01798
5. Schrock, A. B., et al. (2019). Tumor mutational burden is predictive of response to immune checkpoint inhibitors in MSI-high metastatic colorectal cancer. Annals of Oncology.DOI:10.1093/annonc/mdz134