强强联合,免疫治疗新思路
【2019-05-31】
经历了2018年K药和O药在国内上市、诺贝尔生理学或医学奖授予CTLA-4和PD-1的发现者美国科学家詹姆斯·艾利森和日本科学家本庶佑之后,瞬间点燃了大众对免疫治疗的热情。然而,期间也不乏PD-1/PD-L1免疫治疗临床研究失败的消息传来。时至今日,免疫治疗有何新进展?
简说癌症与免疫治疗
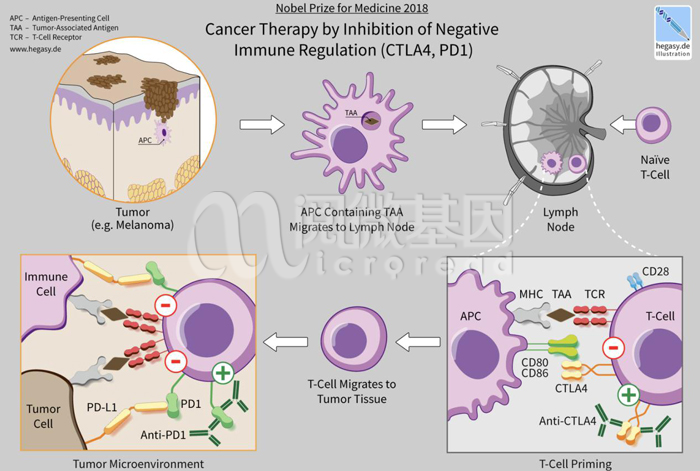
免疫治疗——通过抑制负免疫调节来治疗癌症
正常情况下,免疫系统可以识别并清除肿瘤微环境中的肿瘤细胞,但狡猾的肿瘤君能够采用伪装策略,忽悠过关,使人体免疫系统受到抑制,不能正常杀伤肿瘤细胞,从而在抗肿瘤免疫应答的各阶段得以幸存,也被称为“免疫逃逸”。免疫治疗就是帮助患者堵上自身免疫系统的漏洞,通过增强或恢复抗肿瘤免疫力来杀伤和控制肿瘤。
免疫治疗的发展已经有100多年的历史,肿瘤免疫治疗主要分为免疫检查点抑制剂、过继性免疫细胞、肿瘤疫苗与细胞因子,其中免疫检查点抑制剂治疗以其显著的临床疗效而备受瞩目。
免疫治疗与传统肿瘤治疗方式相比具有以下优势:
· 更广谱的抗癌效果;
· 对癌细胞带有靶向性,更准确,更有效;
· 可抑制癌细胞进化,控制肿瘤,相对来说毒性更低;
· 不损伤反而增强免疫系统;
· 一旦起效,其疗效可维持较长时间,甚至可使晚期癌症病人获得完全缓解进而达到临床治愈。这是免疫药物区别于其它所有药物最大的不同。
免疫检查点抑制剂治疗的现状
免疫检查点是指位于效应T细胞上的一些激活性和抑制性受体调节开关,使用对应配体或抗体可以启动该受体的下游功能(激活或者抑制),激活可使T细胞处于攻击状态,而抑制则使T细胞处于安静状态。人体内有100万亿个种类各异的真核细胞,如何准确地调节T细胞的免疫攻击性能是一个复杂的技术活,牵涉到多种调节机制,免疫检查点便是其中之一。而针对这些受体所开发的抗体药物,包含耳熟能详的CTLA-4抗体和PD-1/PD-L1抗体外,还有LAG-3抗体、TIM-3抗体、TIGIT和VISTA抗体等都属于免疫检查点抑制剂。
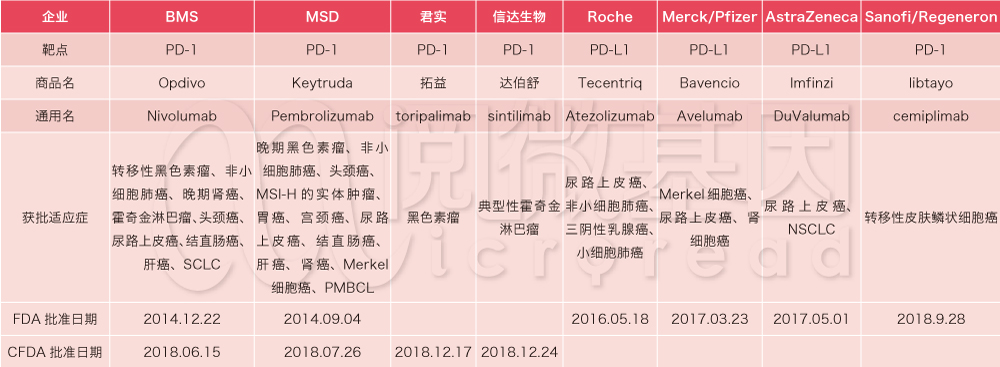
目前美国FDA和中国NMPA批准上市的PD-1/PD-L1抑制剂共有8种,具体情况如下:
免疫治疗面临的挑战
尽管PD-1/PD-L1抗体药物已广泛用于临床肿瘤治疗,但是绝大多数、未经挑选的肿瘤中,PD-1抗体单独使用的有效率仅约10~30%,该如何提高有效率,让免疫治疗服务于更多的患者呢?
对于PD-1/PD-L1抗体疗效的评估,目前已经开发出众多的预测标志物,如PD-L1表达、TMB检测、MSI检测、dMMR检测、TIL检测、肠道菌群分析等,PD-L1和MSI的检测已经在特定癌症的治疗中获得FDA批准,必须根据其检测结果来指导抑制剂的使用。虽然TMB没有正式获得FDA官方批准,但在去年底发布的2019年第一版的非小细胞肺癌NCCN指南中,TMB赫然在列,成为NSCLC患者接受免疫治疗的推荐检测方法。需要重点指出的是,在备注上有明确的提示:作为一个正在演进的biomarker,目前如何对其进行评估还没有形成共识。临床应用中,这些biomarker都各有其不完美之处。
新思路:联合用药解决方案
免疫治疗联合用药应势成为当下肿瘤治疗的新思路,使更多的人群获益于免疫治疗,提高治疗有效率。
目前,Pembrolizumab联合化疗已被FDA批准用于晚期非小细胞肺癌患者一线治疗;atezolizumab联合化疗被批准一线治疗成人广泛期小细胞肺癌(ES-SCLC)患者;atezolizumab联合化疗被批准用于成人无法切除的局部晚期或转移性PD-L1阳性的三阴性乳腺癌(TNBC);双免疫治疗nivolumab联合ipilimumab被批准用于治疗中度或低度风险的先前未治疗的晚期肾细胞癌(RCC)。
今年4月19日,FDA批准PD-1抗体Keytruda(Pembrolizumab)联合Axitinib用于肾癌晚期患者一线治疗。这是首个“PD-1抗体+靶向联合法”获批,也正式开启了“免疫联合靶向”治癌新时代。获批主要依据Keynote-426的大型三期临床试验结果[1]。让我们一起来回顾下Keynote-426的出色表现:
实验入组861名未接受过全身系统治疗的晚期肾细胞癌(RCC)患者。无论PD-L1肿瘤表达状态如何,随机分配432位患者接受Pembrolizumab-Axitinib,429位接受Sunitinib。中位随访12.8个月。主要终点为总生存期(OS)和无进展生存期(PFS),结果显示Pembrolizumab-Axitinib组12个月OS为89.9%,Sunitinib组为78.3%(HR 0.53; 95%CI:0.38-0.74; p <0.0001),中位PFS分别为15.1个月和11.1个月(HR 0.69; 95%CI:0.57-0.84; p = 0.0001)。客观缓解率分别为59.3% (95% CI:54.5-63.9)和35.7% (95% CI:31.1-40.4) (P<0.001)。任何原因的三级及以上不良事件分别为75.8%和70.6%。
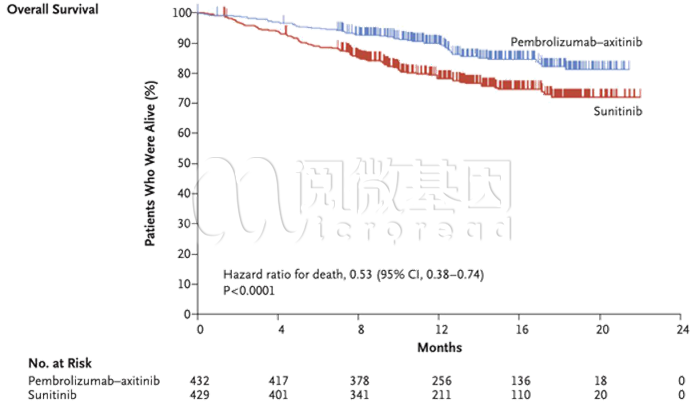
Pembrolizumab-Axitinib组(蓝色)对比Sunitinib组(红色),患者的总生存期
显然,在先前未经系统治疗的晚期RCC患者中,与Sunitinib治疗相比,使用Pembrolizumab-Axitinib联合治疗可显着延长患者总生存期和无进展生存期,并提高客观缓解率。
5月14日,FDA又批准了PD-L1抑制剂avelumab与axitinib联合用于晚期肾细胞癌(RCC)患者的一线治疗。批准主要基于JAVELIN Renal 101的开放性3期试验。相比对照药物,avelumab联合axitinib显著改善了患者中位无进展生存期(PFS)。其中,avelumab联合axitinib的中位PFS为13.8个月,对照药物中位PFS为8.4个月。
联合治疗已成为一种趋势,当然联合治疗也面临着价格昂贵、具有强烈副作用等问题,并不是所有的PD-1/PD-L1抗体联合治疗都能让患者获益。
山重水复,大浪淘沙,未来,我们期待更好的药物组合。
参考文献:
1. Ventola, C. L. (2017). Cancer immunotherapy, part 1: current strategies and agents. Pharmacy and Therapeutics, PMID: 28579724
2. Rini, B. I., et al. (2019). Pembrolizumab plus axitinib versus sunitinib for advanced renal-cell carcinoma. New England Journal of Medicine.
DOI:10.1056/NEJMoa1816714







