一文解答 | MSI/MMR检测3大临床困惑
【2022-02-10】
微卫星不稳定(MSI)作为肿瘤领域炙手可热的Biomarker,可用于林奇综合征筛查、肿瘤预后预测与化疗治疗指导、泛癌种免疫治疗疗效预测。MSI/错配修复(MMR)蛋白检测已被结直肠癌(CRC)、子宫内膜癌(EC)、胃癌(GC)美国国家癌症综合网络(NCCN)指南推荐为所有初诊断患者的常规检测项目,广泛应用于病理与临床科室。但是,MSI/MMR检测在临床应用中,仍存在一些使人困惑的地方,如MSI与MMR的结果不一致、肿瘤的异质性、MMR/MSI检测的质控等。本文聚焦这三大问题,对MSI/MMR进行全面解读。
1. MSI和MMR究竟是啥关系?
微卫星指分布在整个基因组中的短串联重复序列。MSI是由于DNA复制过程中微卫星重复单元出现插入或缺失,且MMR系统无法纠正这些错误而导致的微卫星长度的变化。错配修复系统缺陷(dMMR)是MSI的主要原因。
2. MSI与MMR结果不一致,可能有哪些原因?
研究显示,MMR-IHC与MSI-PCR具有90%-97.5%的一致性。但取样、判读、MMR的异质性染色、新辅助治疗及MMR的功能补偿等原因均可能导致MSI与MMR结果不一致。
(1)错配修复系统正常(pMMR)/微卫星高度不稳定(MSI-H)
①在MMR蛋白的异质性表达区中,MMR蛋白阳性表达的肿瘤也可能存在MMR基因突变及甲基化,表现为MSI-H。
②当编码MMR蛋白的基因发生错义突变时,MMR蛋白功能出现异常但可能并不影响其抗原结构,在这种情况下,IHC是能够检测到MMR蛋白的表达,但其错配修复功能是异常的,MSI的检测结果为MSI-H。
③由于MMR涉及但不限于MLH1、MSH2、MSH6、PMS2、MSH3、PMS1等一系列基因,免疫组化(IHC)未检测的MMR基因突变或尚未识别的MMR基因突变可能导致MMR缺陷,表现为MSI-H[1]。
④有文章报道POLE基因核酸外切酶区域的突变可以解释<1%的pMMR/MSI-H现象[2]。
(2)dMMR/微卫星稳定(MSS)
①由于MMR系统存在功能补偿,使MSS状态不变。常见的补偿机制为PMS2和PMS1互补,MSH6和MSH3互补。最常见的不一致是MSH6表达缺失与MSS状态共存。
一部分原因源于MSH3对MSH6蛋白的功能补偿。当MSH6蛋白受损时,MSH2/MSH3继续工作,DNA错配修复被纠正。
同时由于MSH6主要识别单碱基的错配,使用双核苷酸位点的MSI标记对MSH6的缺陷可能会发生漏检,因此建议使用仅含单核苷酸位点的标记,以便最大限度提高MSH6携带者的检出率[3]。
②新辅助放化疗后的直肠癌可能几乎完全丧失MSH6染色或仅有核仁染色;新辅助放化疗后约30%的直肠癌出现PMS2染色减弱,表现为MSS。此时如果染色模棱两可,取放化疗前的活检标本进行 IHC 染色通常可以解决这个问题[4]。
③有文章报道MLH1启动子的甲基化或MLH1基因的致病性突变可以解释多数MLH1蛋白缺失且MSS的现象[2]。
3. MSI/MMR检测的肿瘤异质性
肿瘤异质性是指观察到不同的肿瘤细胞可以表现出不同的形态和表型特征,包括细胞形态、基因表达、代谢、增殖和转移潜能。这种现象既发生在肿瘤之间(肿瘤间异质性),也发生在肿瘤内部(肿瘤内异质性)。
肿瘤内异质性是指肿瘤内的细胞由于分子变化和克隆选择的逐步累积所驱动的癌症发展过程而具有高度多样性,肿瘤间异质性是指患者体内或不同患者肿瘤间的分子改变。
关于肿瘤异质性的文章大多集中在常见突变上,而关于MSI或MMR检测瘤内和瘤间异质性及其在肿瘤生长过程中可能的变异方面的数据很少。
(1)MMR的异质性表达
MMR的异质性表达在CRC和EC中均有报道,这些肿瘤大多含有弱染色区或无染色区,混合有强染色区和弥漫性染色区。MMR的异质性表达模式包括腺体内型、克隆型和区室型[5],不同类型可以在同一肿瘤中同时存在。其原因不同于由于组织固定、前处理等技术原因引起的IHC染色不均,而具有特定的分子病理机理和意义。
异质性的表达可能和MLH1启动子的异质性甲基化[6-7]、MMR的错义突变甚至是截断突变导致蛋白功能有所保留,这在Lynch 综合征(LS)病例中更频繁地发生(Mangold等人[8]报道,34%的MLH1种系突变携带者的肿瘤显示弱或部分MLH1染色。可能的原因是在所有MLH1致病性突变中,超过三分之一是错义突变[9])以及MSH6的C8重复的次级不稳定[10]等原因相关。
值得注意的是,异质性的染色模式中63%显示肿瘤染色比对照弱,37%显示弥漫性的强染色。肿瘤染色弱于对照的病例肿瘤细胞染色百分比从10%至>95%[9]。
总之,MMR蛋白的异质性染色模式可能导致对结果的错误解释。这也是常规病理实验室只进行IHC检测的主要风险,即把局灶性、异质性或弱染色模式错判为pMMR。因此强烈建议使用MSI和MMR同时检测。
(2)MMR/MSI原发灶与转移灶之间的异质性
MSI/MMR与免疫微环境相关,尽管已经明确了MSI-H肿瘤独特的免疫微环境特征,但是原发性和转移性病灶的MSI状态尚未得到充分探索。LS NCCN指南建议对于转移性的CRC(肝、淋巴结以及其他的转移)在原发肿瘤不可获取的情况下,可以使用转移组织检测MMR。建议主要依据Sigurdis Haraldsdottir 等人的研究[11],50例 dMMR 的原发性 CRC和转移组织的MMR结果完全一致。
尽管原发灶与转移灶之间MSI/MMR 状态高度一致,但是仍有差异被发现。2019年来自中山大学肿瘤中心的何文卓等人的研究团队,发表在Journal of the National Comprehensive Cancer Network的研究[12]显示,19.6% MSI-H的原发性CRC具有MSS转移性肿瘤。
值得注意的是,在肝脏、肺、远处淋巴结转移的患者中,未观察到MSI状态的差异。而在腹膜、卵巢部位都有MSS转移,且4名卵巢转移患者都有MSS转移。MSI状态的不一致率更可能和转移部位存在相关性(P<0.001),而与患者年龄、性别、原发肿瘤位置以及同时与异时转移之间没有显著关联。
作者同时做了一项汇总分析,与其他部位的转移相比,发生腹膜转移或卵巢转移的 dMMR/MSI-H原发肿瘤患者的原发部位和转移部位之间的 MMR/MSI 不一致率更高。
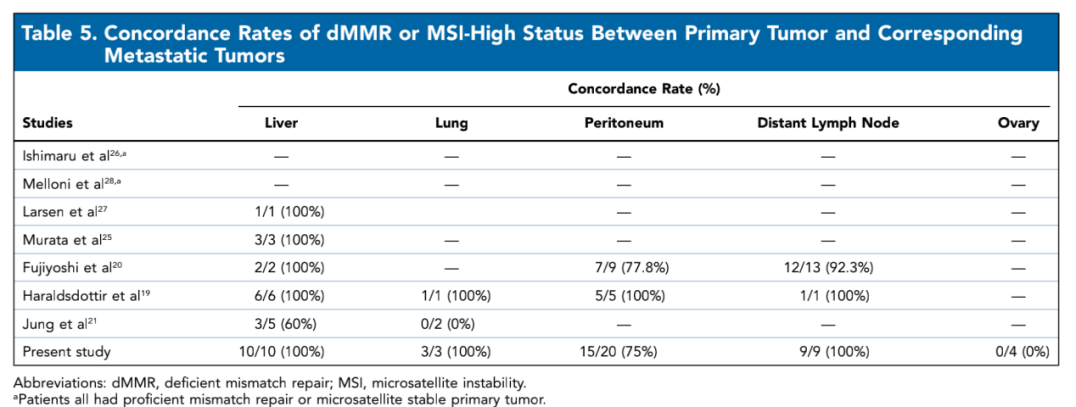
原发性肿瘤和相应转移性肿瘤之间 dMMR /MSI-H的一致性
(3)LS相关同时性及异时性肿瘤的异质性
LS 个体易患同时性和异时性的LS相关肿瘤(LSANs),但MSI/MMR在同时/异时肿瘤中的应用尚未被充分研究。
2016年,Rachel M等人发表在American Journal of Clinical Pathology 的研究[13]显示:69%的患者显示所有LSANs肿瘤间的MMR结果一致,31% 显示肿瘤间MMR结果不一致。
可能的原因是LS 患者也可能通过染色体不稳定途径发展为散发性肿瘤,但发生率尚不清楚。因此如果仅筛查出具有pMMR表达的LSAN,则有31%的病例漏诊了LS诊断,建议如果既往肿瘤是pMMR,则需要考虑在患有同时/异时性肿瘤的个体中筛查所有的同时及异时性LSANs。
4. MSI/MMR检测的质控
2017年FDA批准Keytruda 用于泛癌种的MSI-H/dMMR 晚期患者,尽管免疫检查点抑制剂在MSI-H/dMMR的患者中具有高反应率和持久的临床获益,但仍有10%~40% dMMR/MSI-H mCRC显示免疫治疗的原发耐药。
根据一项发表在JAMA 杂志上的研究[14],MSI和dMMR状态的误诊可能解释了mCRC患者对免疫治疗的原发抵抗。影响MMR检测结果有多方面,所以应建立严格的质控环节,包括严格的试验及结果判读。
(1)MMR检测的质控
目前MMR的判读并没有统一的标准,文献中认为完整MMR染色的阳性判断值范围从任何令人信服的染色、1%、5%到10%不等。无论cut off值是多少,一个关键因素是对染色强度的评估,肿瘤细胞核的MMR染色必须等于或强于内部对照才能被认为是“完整的”[9]。
实际工作中,由于技术问题及不寻常的染色模式,IHC的染色结果可能出现各种误判。IHC染色结果的受多因素的干扰,包括:细胞浆染色、内对照细胞染色弱甚至无染色、肿瘤细的异质性、特殊的病理形态表现、新辅助放化疗、检测样本和罕见染色模式等[15]。
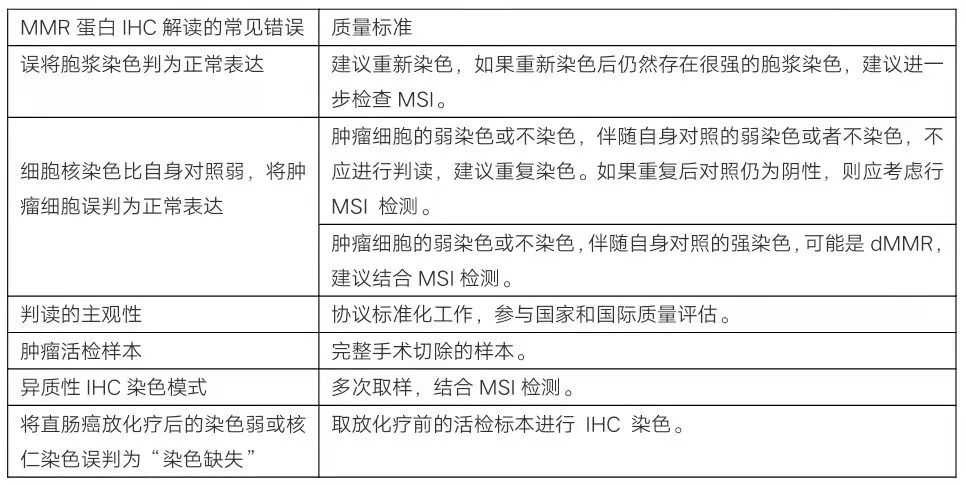
MMR的常见错误及质量标准[15-16]
(2)MSI检测的质控
2011年CAP室间质评数据显示:共有88个独立实验室参与了MSI的室间质评,结果只有78%的实验室正确识别了MSI阳性标本[17],其原因包括缺少标准化的SOP及质控流程、使用敏感性更低的双核甘酸Panel等。
MSI的检测的金标准方法为PCR-毛细管电泳法,检测位点包括1997年NCI推荐的2B3D位点以及包括BAT-25、BAT-26、NR-21、NR-22、NR-24、NR-27、MONO-27在内的5~7个单核苷酸位点Panel。鉴于单核苷酸位点更高的灵敏度与特异性,2004年修订版NCI、NCCN、ESMO、ACMG指南以及国内的专家共识均优先推荐单核苷酸位点。
根据美国病理学会(CAP)室间质评数据显示,2012年单核苷酸位点Panel的使用率超七成[17]。目前国内多个处于临床注册流程的MSI检测试剂盒也采用了单核苷酸位点,表明单核苷酸位点是临床和行业的共同选择。
相比于MMR IHC检测,MSI PCR检测通过设置对照样本、防污染位点、防污染体系等可以建立标准化的质控流程。另外相比于双核苷酸位点,单核苷酸位点具有单态性、出峰简单的特点,可以建立自动化的判读标准。自动化大大减少了分析时间,并可能减少观察者之间和实验室之间的差异。
综上,MMR 可能受技术原因、机理原因及判读原因等多方面的干扰,造成阴性或假阳性结果。MSI则具有易于标准化和自动化的特点。在多种情景下,MMR和MSI可相互补充。为了提高检测准确性,不管在LS的筛查、肿瘤患者治疗指导及免疫检查点抑制剂治疗前,都建议使用MMR和MSI进行联合检测。
本文首发:医学界病理频道
本文作者:王盼盼
题图来源:pixabay
参考文献:
1. Shia J.(2008).Immunohistochemistry versus microsatellite instability testing for screening colorectal cancer patients at risk for hereditary nonpolyposis colorectal cancer syndrome. Part I. The utility of immunohistochemistry. J Mol Diagn.Doi: 10.2353/jmoldx.2008.080031.
2. Stelloo E, et al.(2017). Practical guidance for mismatch repair-deficiency testing in endometrial cancer. Ann Oncol. Doi: 10.1093/annonc/mdw542.
3. Wu Y,et al.(1999). Association of hereditary nonpolyposis colorectal cancer-related tumors displaying low microsatellite instability with MSH6 germline mutations. Am J Hum Genet. Doi: 10.1086/302612.
4. Markow M,et al.(2017). Immunohistochemical Pitfalls: Common Mistakes in the Evaluation of Lynch Syndrome. Surg Pathol Clin. Doi: 10.1016/j.path.2017.07.012.
5. Joost P, et al. (2014).Heterogenous mismatch-repair status in colorectal cancer.Diagn Pathol. Doi:10.1186/1746-1596-9-126
6. Pai RK, et al.(2015). Abrupt loss of MLH1 and PMS2 expression in endometrial carcinoma: molecular and morphologic analysis of 6 cases. Am J Surg Pathol. Doi: 10.1097/PAS.0000000000000415..
7. Kato A, et al.(2016). Isolated Loss of PMS2 Immunohistochemical Expression is Frequently Caused by Heterogenous MLH1 Promoter Hypermethylation in Lynch Syndrome Screening for Endometrial Cancer Patients. Am J Surg Pathol. Doi: 10.1097/PAS.0000000000000606.
8. Mangold E,et al.(2005). Tumours from MSH2 mutation carriers show loss of MSH2 expression but many tumours from MLH1 mutation carriers exhibit weak positive MLH1 staining .J Pathol.Doi: 10.1002/path.1858.
9. Chen W, et al.(2020). Unexpected expression of mismatch repair protein is more commonly seen with pathogenic missense than with other mutations in Lynch syndrome. Hum Pathol. Doi:10.1016/j.humpath.2020.07.001
10. Graham RP, et al.(2015). Heterogenous MSH6 loss is a result of microsatellite instability within MSH6 and occurs in sporadic and hereditary colorectal and endometrial carcinomas. Am J Surg Pathol.Doi: 10.1097/PAS.0000000000000459.
11. Haraldsdottir S,et al.(2016). Mismatch repair deficiency concordance between primary colorectal cancer and corresponding metastasis. Fam Cancer. Doi: 10.1007/s10689-015-9856-2. PMID: 26666765.
12. He W Z , et al.(2019). Comparison of Mismatch Repair Status Between Primary and Matched Metastatic Sites in Patients With Colorectal Cancer. Journal of the National Comprehensive Cancer Network. Doi:10.6004/jnccn.2019.7308.
13. Rachel M. et al.(2016). Discordant Mismatch Repair Protein Immunoreactivity in Lynch Syndrome–Associated Neoplasms: A Recommendation for Screening Synchronous/Metachronous Neoplasms,American Journal of Clinical Doi:10.1093/ajcp/aqw067
14. Cohen R, et al.(2019). Association of Primary Resistance to Immune Checkpoint Inhibitors in Metastatic Colorectal Cancer With Misdiagnosis of Microsatellite Instability or Mismatch Repair Deficiency Status.JAMA Oncol. Doi:10.1001/jamaoncol.2018.494.
15. 高显华, 张卫, 白辰光. 免疫组化筛查林奇综合征的缺陷和应对策略[J]. 中华结直肠疾病电子杂志, 2019.
16. Evrard C,et al.(2019). Microsatellite Instability: Diagnosis, Heterogeneity, Discordance, and Clinical Impact in Colorectal Cancer.Cancers (Basel). Doi:10.3390/cancers11101567.
17. Vasalos P,et al.(2014). Summary of microsatellite instability test results from laboratories participating in proficiency surveys: proficiency survey results from 2005 to 2012..Arch Pathol Lab Med. Doi.10.5858/arpa.2013-0159-CP.






