
基于重亚硫酸盐的甲基化分析方法
简介
生物体可遗传的表型除受DNA 序列的影响以外,还受DNA 甲基化修饰、组蛋白修饰、染色质空间排列等因素的影响。这些不依赖于改变DNA 序列而决定生物性状的遗传方式称之为表观遗传。全基因组重亚硫酸盐测序(Whole genome bisulfite sequencing, WGBS)是基于重亚硫酸盐的甲基化分析方法。首先通过重亚硫酸盐对样本DNA 进行处理,将未甲基化的C 碱基转化为U 碱基,而甲基化的C 碱基保持不变,再结合高通量测序技术,绘制单碱基分辨率的全基因组DNA 甲基化图谱。随着研究的深入,DNA 甲基化在生物发育与疾病发生过程中的调控机制日益清晰,调控网络日益完善,这也对甲基化的研究提出了更高的要求:全面、单碱基分辨率,结合多组学联合分析完善并细化调控网络等。
技术路线
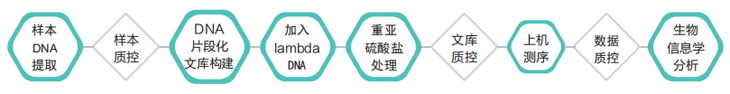
技术优势
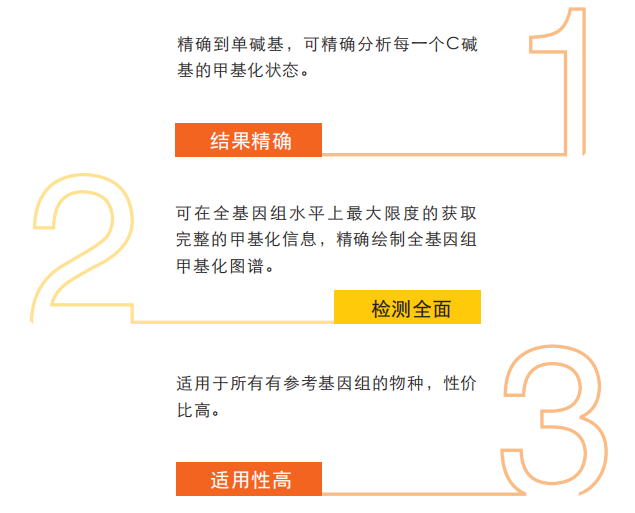
测序策略

收样要求

您能获得的数据
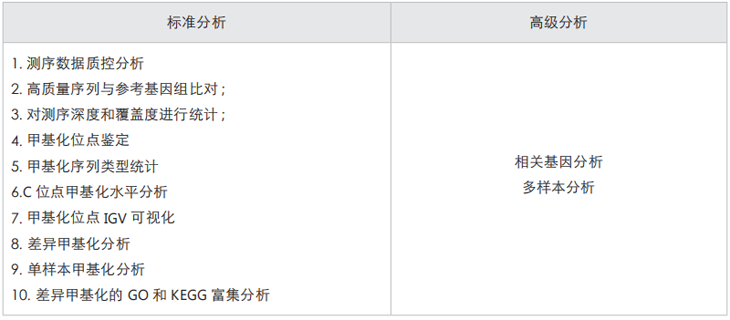
案例解析
培育蜂后:运用表达检测和表观遗传分析
对蜜蜂蜂后发育途径进行研究
在蜜蜂中,蜂后和工蜂被定义为两种不同的社会阶层。蜂后和工蜂分别拥有许多不同的形态学和行为学上的特异性特征,从而保证蜂后极强的生育能力,保证工蜂给蜂后生育提供各种支持,且绝大多数情况下工蜂是不育的。工蜂和蜂后的发育并非来自基因序列差异,而是由于提供给幼虫的营养物质和食物数量的不同造成表观遗传差异(主要为DNA 甲基化修饰),从而调控不同的发育途径。
本研究探索移植到王台的不同年龄工蜂的DNA 甲基化、基因表达与蜂后表型之间的联系,从而解析相关具体机制。研究人员分别将蜂后产在工蜂蜂房内不超过6 个小时的受精卵以及生长1 天、2 天、3 天大小的工蜂幼虫移植到王台饲养为蜂后(QWE, QWL1, QWL2, QWL3)。在DNA 甲基化实验中,分别从王台中选取培养3 天的QWE、QWL1、QWL2,以及一直在工蜂蜂房培养的3 天大小的工蜂幼虫QWL3,共4 组样品,每组3 个幼虫(生物学重复)共12 个样品。
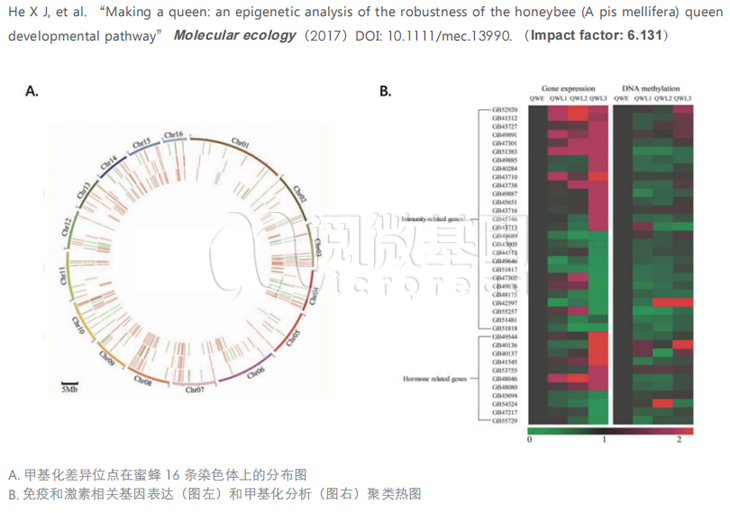
在形态上,QWE 的体型是最大的。就转录组测序结果显示,随着移植时所用工蜂幼虫年龄的增大,差异表达基因数目是增加的。在三个差异分组中,涉及免疫、发育、代谢、生殖能力和寿命的基因在差异表达基因集中都占较大比例。紧接着对四组样品的DNA 进行甲基化测序,结果显示相对于QWE,移植自较大幼虫的蜂后表现出较高的全基因组DNA 甲基化水平。其中,QWE vs QWL3 有146 个差异甲基化区域(DMR),是所有差异分组中DMR 数目最多的,QWE vs QWL1 和QWE vs QWL2 的DMR 数目分别为99 和108 个。分析发现这些基因主要参与一些基础物质的代谢。而在所有3 个差异分组中,DNA 甲基化与基因表达之间呈现非常弱的相关性。同时,还比较分析了参与免疫反应和激素生物合成的基因差异表达与DNA 甲基化间的关系。结果表明,随着移植时所用工蜂幼虫年龄的增大,这些基因表达的差异越明显,但是只有很少一部分基因的DNA 甲基化与基因表达呈现负相关。
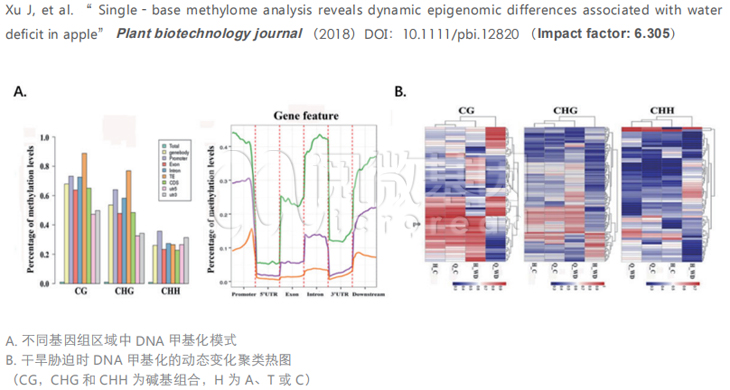
研究趋势及热点
表观修饰的变化广泛的存在于人和动植物内,甲基化的研究主要是研究表观遗传对表型变化的影响以机制:
1. 研究动植物的生长发育:如不同生长发育阶段,不同生长时期和不同组织等。
2. 研究动植物对环境胁迫的应答:如抗寒、抗旱、抗涝等。
3. 研究表观遗传机制。
4. 研究分化衰老机制。
5. 研究疾病发生发展机制:例如癌症导致的基因甲基化等。
常见问题
1. 全基因组甲基化测序有哪些优势?
在全基因组水平达到单碱基分辨率检出甲基化位点,不仅能够高精度发现CpG 岛等常见区域的甲基化水平的变化,还能够分析其他编码基因、基因间区等区域的甲基化水平的差异,分析甲基化对染色体的状态以及基因结构变化的影响,从多维度上解决生物学问题。
2. 哪些物种可以研究WGBS?
要做全基因组甲基化分析,对物种有以下要求:
a. 物种为真核生物;
b. 物种具有参考基因组,且参考基因组的质量要至少拼接到scaffold 水平,最好拼接到染色体水平;
c. 具有较为完整的注释(包含基因水平,有外显子、内含子和CDS 区域等)。
3. 做完全基因组甲基化测序,有哪些方法可以对结果进行验证?
甲基化位点验证可以分为以下几种方法:包括甲基化特异性PCR(MSP)、亚硫酸氢盐测序法(BSP)、质谱法(MassArray)、高分辨率溶解曲线法(HRM)和荧光定量PCR 等。
4. 全基因组甲基化测序需不需要生物学重复?
生物学重复的设计不仅能够排除个体差异对测序结果的影响,在相同的测序深度上,包含DMR 数目、甲基化位点的检出率和正确率等都明显优于没有生物学重复的设计。此外,随着测序成本的下降,技术的发展以及研究的深入,高分文章对实验设计的严谨性要求越来越高,因此生物学重复是十分必要的。






