一文读懂 | 染色体核型分析
【2022-04-14】
核型分析(临床上也常称“染色体检查”)的全称是染色体核型分析。顾名思义,“染色体分析”代表这是一种用于检测染色体异常的遗传学检查项目,“核型”则是指一个体细胞内的全部染色体按其大小、形态特征排列起来构成的图像。所以,染色体核型分析就是检查待检细胞是否存在染色体数目或形态结构异常的检测技术。

G显带核型分析图,图源ISCN
什么时候需要染色体核型分析?
染色体核型分析是遗传学科学研究和辅助临床诊断的重要手段之一,是分析染色体易位、缺失,诊断各种遗传病变的关键指标,并可为细胞遗传分类、物种间亲缘关系以及染色体数目和结构变异的研究提供重要依据。

图源网络
核型分析技术在临床、工业及科研领域均有广泛的应用,其中又以临床应用最为普遍。染色体数目或结构异常会引起染色体疾病,可导致智力低下或发育畸形、不良孕产史等,因此,染色体检查对优生优育非常重要。高龄孕产或有不良产检指征的孕妇会根据医生建议安排胎儿羊水染色体检查,而国内多数生殖医学中心也已将染色体检查纳入试管婴儿治疗前的常规项目。除此之外,其在临床血液病检验项目中也占有非常重要的地位。
在工业领域,传统细胞制品的应用范围不断扩大,细胞治疗和干细胞企业更是蓬勃发展,为使行业规范发展,监管部门陆续颁布了各项政策及指导原则。《中华人民共和国药典》要求,新建人二倍体细胞株及其细胞库必须进行染色体检查,含有活细胞的制品或下游纯化工艺不足的制品也应对所用细胞进行染色体检查及评价。2021年8月,CDE发布了关于公开征求《人源性干细胞产品药学研究与评价技术指导原则(征求意见稿)》意见的通知,建议使用染色体核型分析进行干细胞产品传代稳定性及质量研究。
在科研领域,核型分析则可为细胞遗传分类、物种间亲缘关系的研究提供重要依据。
欲知结果 且说原理
细胞中的遗传物质平时是以染色质的形式存在,只有在细胞分裂时染色质才会浓缩成染色体的形态。细胞有丝分裂又分为了间、前、中、后、末几个阶段:间期是遗传物质的准备及复制;前期核仁消失染色质浓缩成染色体,纺锤体出现;中期纺锤体移至细胞两极,染色体在赤道面上排列;后期姐妹染色单体在纺锤丝的牵引下分开并移向两极;末期子细胞形成。因此,分裂中期的染色体是最便于观察的。
染色体之所以叫“染色”体,跟它便于被碱性染料染色有关,而不同的染料产生的染色效果也有明显差异。
通过是否经过显带技术处理,可将染色分为非显带染色和显带染色,未经特殊处理,直接染色后镜下观察进行核型分析的过程称为染色体非显带核型分析;而标本经显带技术处理后,会使染色体沿纵轴上显示出一定数量的、着色程度不同、宽窄不等的明暗相间的带纹。每条染色体都有独特而恒定的带纹,通过与标准带形图对比就可达到识别分析染色体形态、结构的目的。
ISCN与常用染色体显带技术的发展
1956年,蒋有兴和Levan首次报道人类染色体数目为46条,激发了人们对细胞遗传学的兴趣;1959年,多家实验室分别提出了染色体的分类和命名方法;1960年召开的“丹佛会议”提交了名为“关于人类有丝分裂染色体命名标准体系”,这一体系也是之后所有命名体系的基础。
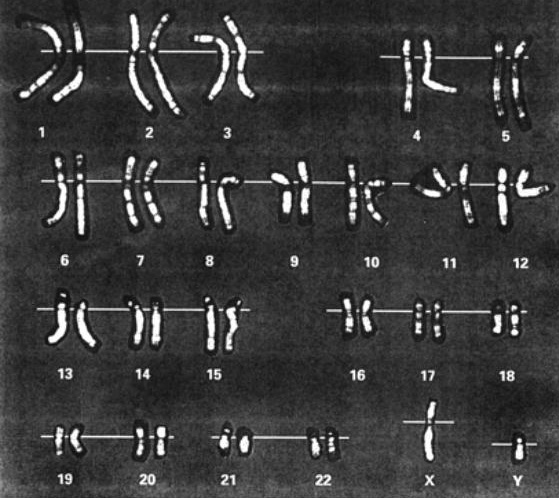
Q带染色图,图源ISCN
1968年,瑞典学者Torbjom Caspersson及其同事发表了第一张植物染色体显带照片(二氢盐酸喹吖因染色),这是细胞遗传学领域第二个重大的突破。该小组迅速把他们的研究推广到人类染色体,并且于1970 年发表了第一张人类染色体显带核型照片。很快,其它的几种染色体显带技术也被发明出来。这时人们认识到,由于每条人类染色体都能通过现代技术得到准确的辨认,现存的命名系统不再适用。随后经过几年的发展,最终1977 年在Stockholm召开的会议,将此前的会议报告整理成了一项文件,即为人类细胞遗传命名的国际体制——《人类细胞遗传学国际命名体系(1978)》,简写为ISCN(1978),这一文件包括了关于人类细胞遗传学命名的完整体系。
瑞典学者Torbjom Caspersson报道的使用芥子喹吖因或二盐酸喹吖因产生荧光性带型模式的方法,即Q显带方法。而使用Giemsa的染液染色,可在染色体上产生和Q显带模式基本相同的带型模式,即G显带方法。除此之外,还有可产生与G显带带型模式相反的R带,显示特殊染色体结构的C带(结构性异染色质),T带(端粒)和NORs(核仁组织者区)。其中,G带染色不像Q带会受荧光显色时间短的限制,且在普通显微镜下就可以进行观察,为一般实验室普遍采用。
染色体核型分析检测流程
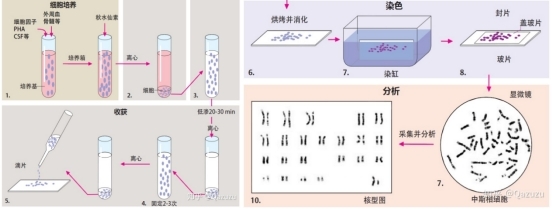
核型分析检测流程,图源知乎
这里以G显带染色为例,可将检测流程归纳为:秋水仙素共培养→低渗处理→固定→制片→染色→显微计数及染色体配对分析。其中秋水仙素可以抑制有丝分裂,破坏纺锤体,使细胞停滞在分裂中期,便于收集到更多的分裂相细胞。低渗处理有利于细胞膨胀,使染色体分散铺展。固定是将组织细胞及其成分选择性的固定于某一特定阶段的过程,在杀死细胞的同时可避免研究成分受到破坏。再经过制片染色就可以上显微镜进行拍照了,后面再根据不同标准,选取条带水平在400-550G的中期分裂相,进行染色体的带型分析,最终形成完整的报告。
染色体条带水平(分辨率)是什么意思?

300、400、550、700 和850 条带水平的单倍体核型,图源ISCN
染色体的条带水平(分辨率)是什么?是不是分辨率越高越好?根据ISCN规定,染色体的条带水平由在单倍体上(22 条常染色体和X、Y 染色体)所见到的带的数目来表示,即在400条带水平下,22 条常染色体和X、Y 染色体中明条带与暗条带的总数为400条。由此看出染色体的条带水平越高,分辨率也就更高,可检出更小的染色体片段。
但一味追求染色体的高分辨率也是不行的,条带水平过高时,染色体上会出现无数细分的线状甚至点状结构,也就不具备特异性的带型模式,在进行分析的时候也会增加对识别和判读的难度,更无法用于诊断。因此ISCN也只提供了300、400、550、700、800的标准显带模式图谱,其在实际应用中已可满足需求。
阅微基因染色体核型分析检测
阅微基因核型分析(G显带法)检测针对不同的客户需要,可分别提供临床规格和药典规格的报告。

左:临床规格报告模板 右:药典规格报告模板
临床规格的报告依据ISCN要求,会选取20个细胞进行核型分析及描述,再选取一张最具代表性的核型排列图进行展示。这一规格适用于初次送检的未知核型细胞或用于内部质控,其主要目的是了解染色体核型状况。
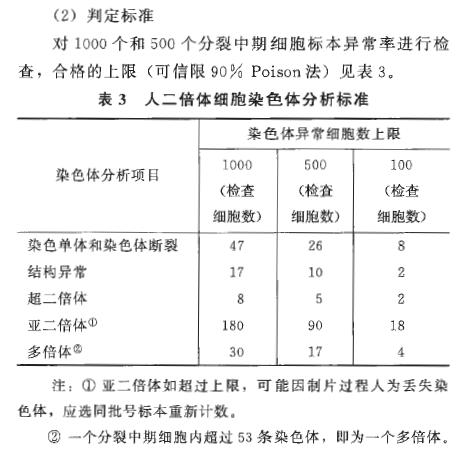
人二倍体细胞染色体分析标准,图源《中国药典》2020版
针对有申报需求的客户可提供三种规格报告。按药典要求对至少50个细胞核型分析,并根据检查细胞数(100、500、1000个)的不同统计异常细胞数是否符合药典要求的上限。报告中也会提供一张最具代表性的核型排列图进行展示。
相对于临床规格,药典规格的检测项目更多也更严格。因此我们建议客户在送检药典规格前,先进行临床规格的检测,排除掉染色体的异常后再送检药典规格,防止出现不合格的情况。尤其是肿瘤来源细胞或细胞系类的样本,是并不适合使用药典方法进行分析的,因为这类细胞通常发生了染色体水平的变异,比如工业领域常用的293T细胞,就是亚三倍体的细胞系,这类细胞会出现多种复杂的核型,其染色体异常细胞数量也必然会超过药典规定。
结语
染色体的核型分析始于1968年的显带技术,至今已有50余年的历史,在这期间随着科技的进步,也不断有新的检测技术涌现,如在20世纪80年代末发展出的荧光原位杂交(FISH),21世纪的SKY光谱染色体自动核型分析,近年来也有将高通量测序方法应用于染色体异常的检测。但FISH会受探针来源的限制,SKY及二代测序难以检测染色体的易位倒位等,而G显带技术则受到分辨率的限制,难以发现染色体的细微变异。对于染色体的核型分析,现有检测方法均有其技术上的局限性,但G显带这一经典方法在临床及工业科研等领域至今仍有着不可替代的地位。
关于核型分析检测的送检要求和更多技术问题,欢迎咨询阅微基因!
参考文献:
[1]《人类细胞基因组学国际命名体系(2016版)》(ISCN2016)
[2] 中华预防医学会出生缺陷预防与控制专业委员会, 张雪梅, 戚庆炜,等. 胎儿染色体核型分析判读指南[J]. 中华医学遗传学杂志, 2021, 38(5):5.
[3] 徐丽霞, 王秦秦. 染色体核型分析技术的发展[J]. 医学综述, 2009, 15(2):3.
[4] 朱晓丹, 李超, 欧妙玲,等. 高通量测序与染色体核型分析技术用于产前诊断的比较分析[J]. 医药前沿, 2021, 11(13):2.







